安心・安全へのこだわり(in vivo,in vitro)
90日間反復経口投与毒性試験
安全性試験の目的
光合成細菌RAP99の反復経口投与による長期間継続的に摂取した場合の有害影響の有無を明らかにするため、ラットを用いて試験を行なった。
方法
結果および考察
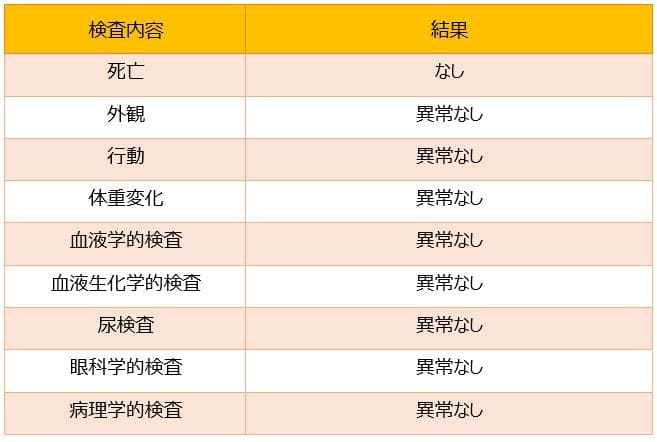
安全性試験の結果は表2の通り
表2に示したとおり光合成細菌RAP99の長期間の継続的食用によるラットへの悪影響はなかった。
以上の結果から、光合成細菌RAP99は限度量※11000mg/kg/dayにおいて毒性影響はないと結論された。
※1 ガイドラインが定める最高用量の事であり、1000mg/kg/dayで何ら毒性影響が認められない場合は、それ以上の投与量で実施する必要はない量を言う。
【薬物安全性試験センター】
ラット骨髄細胞を用いた小核試験
試験目的
ラット骨髄細胞を用いて、RAP99の染色体異常誘発能の有無を明らかにした。
試験方法
RAP99の染色体異常誘発能の有無を検討するため、RAP99を投与した7週齢雄ラットの骨髄細胞を用いて小核試験を実施した。
RAP99の500、1000及び2000 mg/kgを約24時間間隔で2回経口投与し、2回目投与後約24時間に骨髄塗抹標本を作製して観察を行った。本試験は、以下のGLP基準に準拠して行った。
「医薬品の安全性に関する非臨床試験の実施の基準に関する省令」(厚生省令第21号:平成9年3月26日)
試験実施者
株式会社ボゾリサーチセンター
本社:〒151-0065 東京都渋谷区大山町36-7
実施施設・御殿場研究所:〒412-0039 静岡県御殿場市かまど1284
判定基準
以下の全ての条件を満たす時、陽性と判断した。
1) 少なくとも1つの投与群で、小核を有する幼若赤血球(MNPCE)の出現頻度が陰性対照群と比較して統計学的に有意な増加を示している場合。
2) 1)の結果を傾向検定で評価した場合、用量依存性の増加がみられる場合。
試験結果
1.一般状態
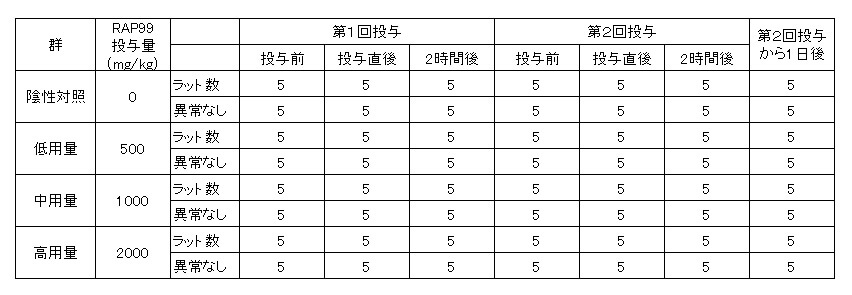
結果を表1に示した。
いずれの群にも死亡はみられず、いずれの動物にも一般状態の変化はみられなかった。
表1 ラットの一般状態観察結果
2.体重
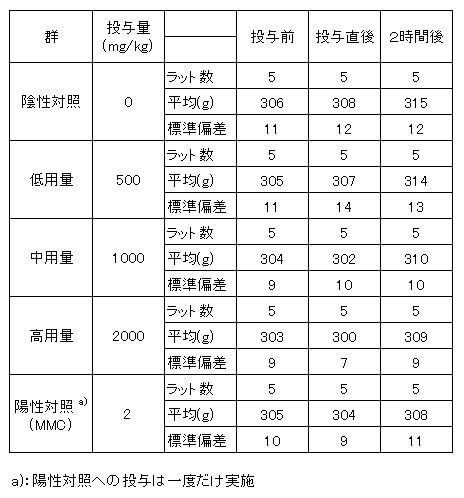
結果を表2に示した。
被験物質投与による体重への影響はみられなかった。
表2 ラットの体重測定結果
3.骨髄塗抹標本の観察結果
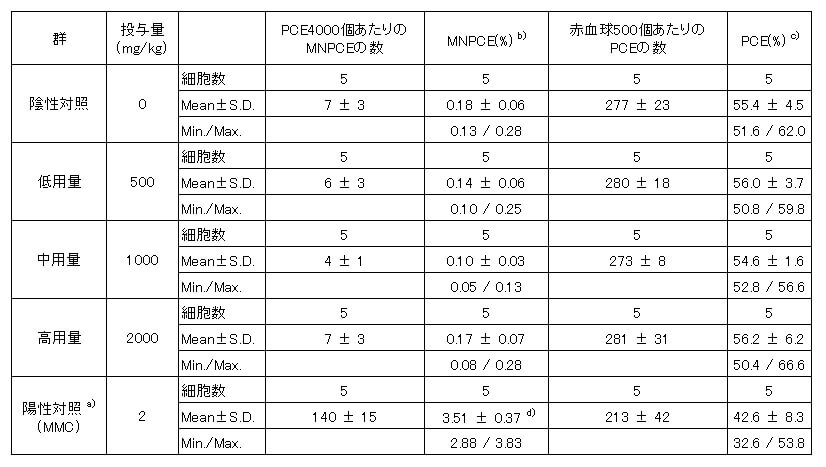
結果を表3に示した。
幼若赤血球(PCE)4000個中に占める小核を有する幼若赤血球(MNPCE)の出現頻度は、500、1000及び2000 mg/kg投与群で、それぞれ0.14% ± 0.06%、0.10% ± 0.03%及び0.17% ± 0.07%であり、陰性対照群の値(0.18 ± 0.06%)と比較して統計学的に有意な増加を示さなかった。
また、各被験物質投与群の全赤血球500個中に占めるPCEの出現頻度は、陰性対照群と比較して統計学的に有意な変化を示さなかった。
表3 骨髄塗抹標本の観察結果
a):陽性対照への投与は一度だけ実施
b):4000個の幼若赤血球(PCE)あたりの小核を有する幼若赤血球(MNPCE)の割合(%)
c):500個の赤血球あたりの幼若赤血球(PCE、MNPCEを含む)の割合(%)
d):陰性対照値からの統計的に有意な増加(フィッシャーの直接確率検定、P <0.05)
陰性対照群と処置群の間に有意差無し
結果・考察
RAP99投与によるラットの一般状態および体重には変化がみられなかった。
また、骨髄塗抹標本を観察した結果、RAP99投与によるMNPCEの出現頻度は統計学的に増加を示さなかった。
以上の結果より、本試験条件下においてRAP99の染色体異常誘発能は陰性であると判断された。
復帰突然変異試験
試験目的
RAP99の遺伝子突然変異誘発能※の有無を明らかにするため、細菌を用いて試験を行った。 ※突然変異とは、生物やウイルスがもつ遺伝物質の質的・量的変化のこと。
また、その変化によって生じる状態のことをいう。突然変異した細胞は腫瘍の発症につながることがある。
試験方法
RAP99の遺伝子突然変異誘発能の有無を検討するため、サルモネラ菌(TA100、TA1535、TA98、TA1537)及び大腸菌(WP2 uvrA)を用いて代謝活性する場合及び代謝活性しない場合の条件化で、Ames試験を行った。
各々0、313、625、1250、2500、および5000μg/プレートの5用量で実施した。 本試験は、以下のGLP基準に準拠して行った。 「医薬品の安全性に関する非臨床試験の実施の基準に関する省令」(厚生省令第21 号:平成9年3月26日)
試験実施者
株式会社ボゾリサーチセンター
本社:〒151-0065 東京都渋谷区大山町36-7
実施施設・東京研究所:〒156-0042 東京都世田谷区羽根木1-3-11
判定基準
被験物質処理群の復帰変異コロニー数の平均値が自然復帰変異コロニー数(陰性対照値)の平均値に対して2倍以上となる増加を示し、用量反応性が認められた場合に陽性と判定した。
試験結果
本試験の結果を以下に示した
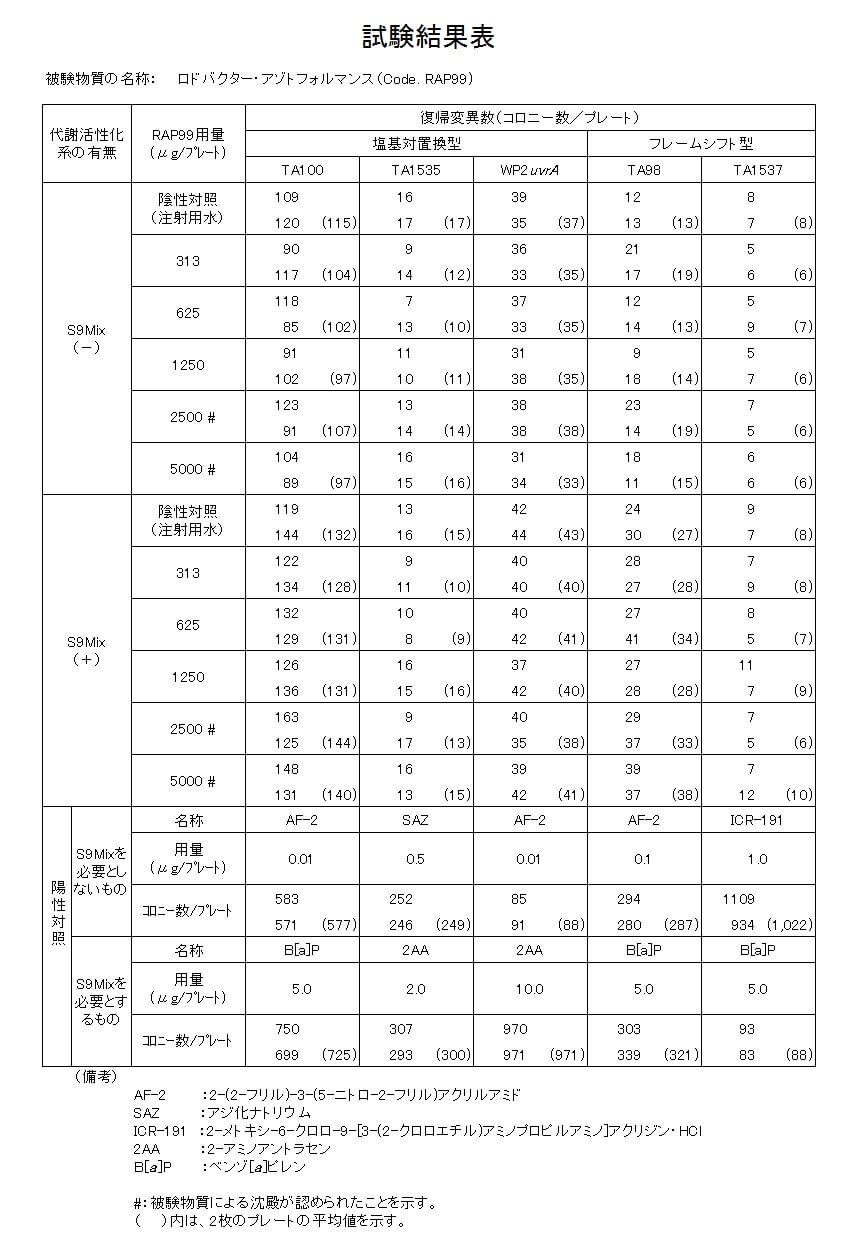
表1 試験結果
(備考)
AF-2:2-(2-フリル)-3-(5-ニトロ-2-フリル)アクリルアミド
SAZ:アジ化ナトリウム
ICR-191:2-メトキシ-6-クロロ-9-[3-(2-クロロエチル)アミノプロピルアミノ]アクリジン・HCl
2AA:2-アミノアントラセン
B[a]P:ベンゾ[a]ピレン
#:被験物質による沈殿が認められたことを示す。
()内は、2枚のプレートの平均値を示す。
結果・考察
代謝活性化の有無にかかわらず、いずれの菌株においても陰性対照値の2倍以上となる復帰変異コロニー数の増加は認められず、用量反応性も認められなかった。
よって、本試験条件下においてRAP99は、細菌に対する遺伝子突然変異誘発能を有さない(陰性)と判定した。